تفاوت های کربنات سدیم با بی کربنات سدیم (جوش شیرین)

کربنات سدیم (Na2CO3) و بی کربنات سدیم (NaHCO3) دو ترکیب شیمیایی مهم هستند که به صورت صنعتی تولید میشوند. این دو ترکیب، در بسیاری از صنایع و کاربردها نقش مهمی را ایفا میکنند. علاوه بر این، هر یک از این ترکیبات دارای خواص و کاربردهای منحصر به فردی هستند که آنها را از یکدیگر تمایز میدهد. هدف از این مقاله، بررسی و مقایسه تفاوت های مهم بین کربنات سدیم و بی کربنات سدیم است. در ادامه، به بررسی خواص فیزیکی و شیمیایی و کاربردهای کربنات سدیم و بی کربنات سدیم پرداخته خواهد شد.
کربنات سدیم و بی کربنات سدیم دو مورد از پرکاربردترین و مهم ترین مواد شیمیایی هستند. هر دو کاربردهای مشترک زیادی دارند. این دو ماده علیرغم شباهت نامشان یکسان نیستند و ویژگی ها و کاربردهای زیادی دارند که تفاوت های زیادی با هم دارند.
تفاوت کربنات سدیم و بی کربنات سدیم در ساختار
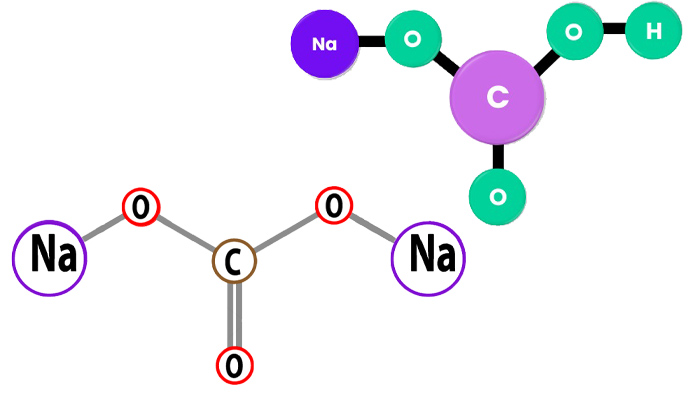
همانطور که گفتیم، از نظر شیمیایی، کربنات سدیم و بی کربنات سدیم بسیار شبیه هستند. فرمول کربنات سدیم Na2CO3 و فرمول بی کربنات سدیم NaHCO3 است. هر دو ترکیبات یونی هستند که وقتی در آب حل می شوند، یون سدیم (Na) با بار مثبت و یون کربنات با بار منفی (CO3) آزاد می کنند. بی کربنات سدیم همچنین شامل یک یون هیدروژن (H) با بار مثبت است. با این حال، این دو ترکیب تفاوتهایی در ساختار و خواص شیمیایی خود دارند.
کربنات سدیم (خاکستر سودا) یک ترکیب معدنی است که به صورت بلورهای سفید یا بیضوی در دسترس است. در ساختار کربنات سدیم، یونهای سدیم (Na⁺) به صورت نسبتاً منظمی در یک ماتریس بلوری قرار دارند. همچنین، یونهای کربنات (CO₃²⁻) نیز ساختاری بلوری دارند و با یونهای سدیم به صورت الکترواستاتیکی ارتباط دارند.
این ساختار بلوری به دلیل وجود پیوندهای قوی بین یونها، مقاومت نسبی دارد و در حالت خالص به صورت بلورهای بزرگ تشکیل میشود. بی کربنات سدیم نیز تا اینجا، درست مانند کربنات سدیم می باشد، اما تفاوت آنها در این مورد است، ساختار بیکربنات سدیم نسبت به کربنات سدیم کمی کمتر پایدار است و در حالت خالص به صورت بلورهای بزرگ تشکیل نمیشود.
بیکربنات سدیم نسبت به کربنات سدیم در مواردی مانند تولید برخی گازها، تنظیم pH، درمان عفونتهای قارچی و غیره کاربردهای بیشتری دارد. همچنین، به دلیل وجود گروه هیدروژن در ساختار بیکربنات سدیم، این ماده میتواند با اسیدها واکنش دهد و دارای خواص آنتی اسید است.
تفاوت کربنات سدیم و بی کربنات سدیم در خواص

بی کربنات سدیم معمولاً یک پودر جامد سفید است. این ماده به راحتی در آب حل می شود و به عنوان یک پایه ضعیف الکترولیتی عمل می کند. کربنات سدیم نیز یک پودر جامد و سفید است. این ماده نیز به صورت پودری تولید می شود و یک ماده قلیایی قوی است. هر دو ماده در تماس با پوست بی ضرر هستند اما می توانند باعث تحریک چشم شوند. در غلظت های پایین، هیچ کدام در صورت مصرف سمی نیستند.
کربنات سدیم و بیکربنات سدیم دارای خواص متفاوتی هستند. در ادامه، برخی از این تفاوتها را بررسی خواهیم کرد:
- pH: یکی از تفاوتهای مهم بین این دو ترکیب، pH آبهای حاصل از آنها است. کربنات سدیم، به دلیل وجود یونهای کربنات (CO₃²⁻) که در آب تفکیک میشوند، قادر به تولید یونهای هیدروکسید (OH⁻) است و باعث افزایش pH محلول میشود. از سوی دیگر، بیکربنات سدیم تنها یک یون هیدروژن کربنات (HCO₃⁻) تولید میکند که به نسبت کربنات سدیم، کمتر قادر به تغییر pH محلول است و خنثی تر است.
- خاصیت آنتی اسید: بیکربنات سدیم دارای خواص آنتی اسید است. این به این معنی است که در حضور اسید، یون هیدروژن کربنات آزاد شده، با اسید واکنش میدهد و در نتیجه pH محلول کاهش مییابد. از این خاصیت برای تنظیم و تعدیل pH در فرایندهای شیمیایی و صنعتی استفاده میشود.
- قابلیت حل در آب: کربنات سدیم و بیکربنات سدیم هر دو قابلیت حل در آب را دارند. با این حال، تفاوت آنها در این است که بیکربنات سدیم نسبت به کربنات سدیم راحت تر و زودتر در آب قابل حل میشود.
تفاوت کربنات سدیم و بی کربنات سدیم در نحوه تولید
کربنات سدیم به طور طبیعی در زمین و منابع معدنی وجود دارد ولی می توان آن را به صورت شیمیایی نیز تولید کرد. کربنات سدیم در سراسر جهان یافت می شود و معادن بزرگی در ایالات متحده، بوتسوانا، چین، اوگاندا، کنیا، پرو، مکزیک، هند، آفریقای جنوبی، مصر و ترکیه دارد. همچنین کربنات سدیم عمدتاً با استفاده از فرآیند Solvay تولید می شود که در آن کلرید سدیم (نمک) و آمونیاک برای ایجاد کربنات سدیم مخلوط می شوند.
بی کربنات سدیم یک ماده شیمیایی است که با پمپاژ آب گرم از بسترهای معدنی تولید می شود. بی کربنات سدیم در آب حل می شود و از محلول متبلور می شود. اما این ماده اکثرا برای مصارف متنوع در کارخانه های استاندارد تولید می شود و روش های مختلفی برای تولید آن وجود دارد.
نحوه شناسایی
کربنات سدیم و بی کربنات سدیم در بازار نام های مختلفی دارند. کربنات سدیم اغلب خاکستر سودا نامیده می شود. نام های دیگر آن عبارتند از: سودای شستشو، نمک دی سدیم اسید کربنیک، کربنات دی سدیم و سودای کلسینه شده. بی کربنات سدیم نیز بیشتر به صورت جوش شیرین یا بیکینگ پودر دیده می شود. همچنین با نام های بی کربنات سودا، نمک مونوسدیم اسید کربنیک، کربنات هیدروژن سدیم و کربنات اسید سدیم نیز دیده می شود.
برای تشخیص کربنات سدیم از بیکربنات سدیم، میتوانید از روشهای آزمایشگاهی و شیمیایی مختلف استفاده کنید. در این بخش، چند روش تشخیص این دو ترکیب آورده شده است:
- استفاده از اسید: با افزودن اسید به نمونه مورد نظر، اگر بیکربنات سدیم در نمونه وجود داشته باشد، گاز کربن دیاکسید (CO₂) آزاد میشود.
- آزمایش با استفاده از اندازهگیری pH: کربنات سدیم باعث افزایش pH محلول میشود.
- آزمایش با استفاده از اندازهگیری وزن مولکولی: وزن مولکولی کربنات سدیم (Na₂CO₃) بیشتر از بیکربنات سدیم (NaHCO₃) است.
فواید و کاربردها

بی کربنات سدیم که بیشتر به عنوان جوش شیرین دیده می شود، کاربردهای خانگی بسیار متنوعی دارد. این ماده یک بخش ضروری در پخت و پز کیک و نان است، بو را کاهش می دهد، می تواند برای تمیز کردن استفاده شود و به عنوان یک خاموش کننده آتش نیز عمل می کند. بی کربنات سدیم نیز یک ماده پرکاربرد در داروسازی برای کاهش اسیدیته به خصوص در معده است. اما رایج ترین کاربرد کربنات سدیم در تولید شیشه است. سایر کاربردهای کربنات سدیم شامل فرآوری شیمیایی و ساخت صابون است. پس رایجترین کاربردها و فواید این دو ترکیب به این صورت است:
کربنات سدیم (Na₂CO₃):
- تولید شیشه: به عنوان یکی از مواد اصلی در تولید شیشه استفاده میشود. این ترکیب موجب افزایش دمای ذوب شیشه میشود و در فرایند تصفیه و از بین بردن اثرات آهن و سایر آلایندهها نیز مؤثر است.
- تولید صابون و مواد شوینده
- تنظیم pH
- صنعت نساجی: کربنات سدیم در فرایند رنگرزی و پردازش الیاف نساجی استفاده میشود. این ترکیب موجب تثبیت رنگ در الیاف و افزایش ثبات رنگ میشود.
- و غیره
بیکربنات سدیم (NaHCO₃):
- خمیر دندان: بیکربنات سدیم در تهیه خمیر دندان استفاده میشود. این ترکیب قادر به جذب بو و طعم نامطبوع است و به عنوان مادهای ضد عفونی کننده نیز عمل میکند.
- تنظیم pH
- آشامیدنی: بیکربنات سدیم در تهیه نوشیدنیها و آب معدنی استفاده میشود. این ترکیب به عنوان یک ماده ضد سوزش معده عمل میکند.
- آشپزی
- و غیره




